ポリマーに機能を加え 医療のツールに
物質生命科学科
小土橋陽平 准教授
小土橋陽平 准教授

「温度で性質が変わる」「光を当てると光る」「細菌を吸着し倒す」――。こうした付加機能を持ったフィルムやプラスチックがあれば、より便利で有益な製品を作り出すことができるでしょう。
物質生命科学科の小土橋陽平准教授は、フィルムやプラスチックの素材となるポリマー(※1)に機能を付け加えたり、機能を持ったポリマーを有益に使ったりする研究を進めています。ポリマーと同義の用語として「高分子」を用いることが多いので、以下、ポリマーを高分子、機能を持ったポリマーを「機能性高分子」と表記することにします。
※1 ポリマー:複数のモノマーが重合してできた化合物。一般的には分子量が大きな有機化合物である。一方、「高分子」も分子量が大きなポリマーを指す用語であるため、ポリマーと同義で用いられることが多い
機能を発揮する分子構造を見つけたとしても、それを高分子に組み込むとなると、一般には複雑な化学合成を経ることになるのではないかと想像してしまいます。ですが、小土橋准教授の研究を見ると、実にスマートな方法を編み出していることに驚かされます。まずはその「鮮やか」ともいえる研究成果を見ていきましょう。
物質生命科学科の小土橋陽平准教授は、フィルムやプラスチックの素材となるポリマー(※1)に機能を付け加えたり、機能を持ったポリマーを有益に使ったりする研究を進めています。ポリマーと同義の用語として「高分子」を用いることが多いので、以下、ポリマーを高分子、機能を持ったポリマーを「機能性高分子」と表記することにします。
※1 ポリマー:複数のモノマーが重合してできた化合物。一般的には分子量が大きな有機化合物である。一方、「高分子」も分子量が大きなポリマーを指す用語であるため、ポリマーと同義で用いられることが多い
機能を発揮する分子構造を見つけたとしても、それを高分子に組み込むとなると、一般には複雑な化学合成を経ることになるのではないかと想像してしまいます。ですが、小土橋准教授の研究を見ると、実にスマートな方法を編み出していることに驚かされます。まずはその「鮮やか」ともいえる研究成果を見ていきましょう。
機能を組み込む自在な発想
なじみのある高分子にPVA(ポリビニルアルコール)があります。食品包装用フィルムや液晶パネル(の偏光板)など身近な商品に幅広く使われている材料ですが、構造上、新たな機能を付加しづらい材料です。付加する方法として知られているのは、有機反応や紫外線処理などの工程を複数回繰り返す、高コストな方法でした。

PVAに高分子を結合させる
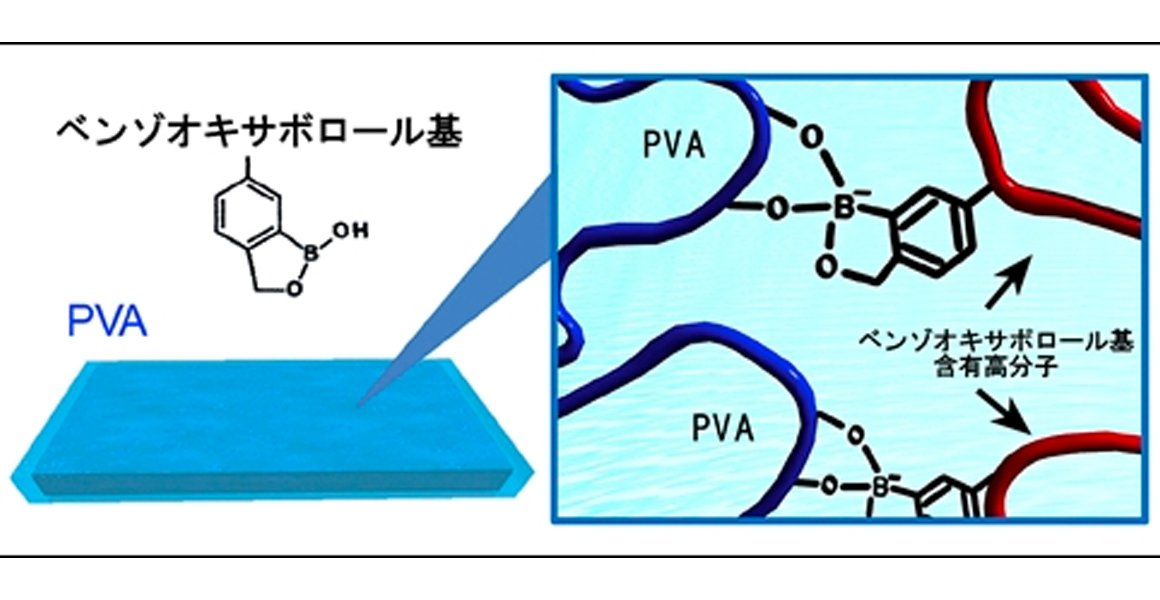
ベンゾオキサボロール基を持たせれば、機能性高分子を
PVA(ポリビニルアルコール)に付けられる
小土橋准教授は、PVA(のジオール基)と共有結合するベンゾオキサボロール基に着目しました。ベンゾオキサボロール基を持った高分子であればPVAに結合することができるのです。そこで小土橋准教授は、ベンゾオキサボロール基を含んだ機能性高分子を用意し、これをPVAに混入することで結合させ、PVAに機能を持たせることに成功しました。
この結合は可逆的な(つまり条件を変えることで離すこともできる)弱い結合ですが、PVA分子そのものを改変するよりシンプルでコストのかからない方法です。実験では実際に、温度応答性やpH応答性といった機能を備えたPVAフィルムを作りました。
この結合は可逆的な(つまり条件を変えることで離すこともできる)弱い結合ですが、PVA分子そのものを改変するよりシンプルでコストのかからない方法です。実験では実際に、温度応答性やpH応答性といった機能を備えたPVAフィルムを作りました。
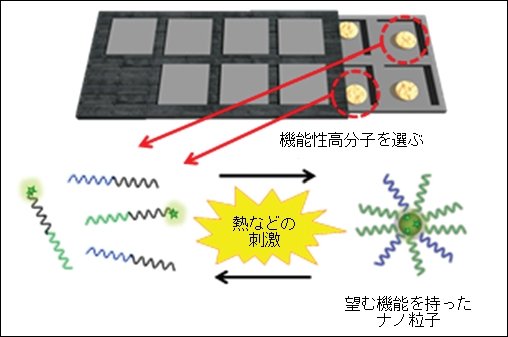
望むナノ粒子が出来るまで
小土橋准教授はこの方法でがん組織に集まり光るナノ粒子を作った。血液など他の細胞に対して悪影響を及ぼさないこと、そして役目を終えたナノ粒子はバラバラになって腎臓から尿として排出されることも確認した
また小土橋准教授は「ナノ粒子キット」という、複数の機能性高分子を自由に組み合わせる手法も開発しました。例えば、体内に入れるとがん組織に集まり光るナノ粒子が欲しいとします。その場合は、がん細胞に集まる機能性高分子と光る機能性高分子を選び、水に溶かして体温まで加温します。すると高分子同士が集合します。これでがん細胞だけを選択的に光らせる粒子の出来上がりです。つまり、熱を加えると集合する分子配列部分を持った機能性高分子を用意しておけば、希望する機能の組み合わせが簡単にできるのです。まるでレゴブロックのようなキットです。
薬剤耐性菌に立ち向かう
ナノ粒子キットの研究を見ていくと、アプローチのスマートさが理解できると思います。また同時に、小土橋准教授が目指している目標も見えてくるのではないでしょうか。「私たちの研究室では、医療に役立つ機能性高分子の開発を進めています」。
小土橋准教授が2016年に本学に着任してから注力している研究テーマに、抗菌機能を持つ傷口の被覆材(ドレッシング材)があります。ドレッシング材とは、いわば絆創膏(ばんそうこう)のようなものですが、研究で想定しているのは手術後の傷口を覆うなど主に医療の現場で利用されるドレッシング材です。
開発に駆り立てたものは、人類にとっての脅威「薬剤耐性菌」による死者の増加です。米国では年間3.5万人以上、欧州では年間3.3万人が死亡していると推定されています。対策を採らないと2050年には世界で1000万人が薬剤耐性菌に関連して亡くなるという予測があるほどです。抗生物質がすぐに効かなくなる薬剤耐性菌は深刻な問題なのです。
小土橋准教授が2016年に本学に着任してから注力している研究テーマに、抗菌機能を持つ傷口の被覆材(ドレッシング材)があります。ドレッシング材とは、いわば絆創膏(ばんそうこう)のようなものですが、研究で想定しているのは手術後の傷口を覆うなど主に医療の現場で利用されるドレッシング材です。
開発に駆り立てたものは、人類にとっての脅威「薬剤耐性菌」による死者の増加です。米国では年間3.5万人以上、欧州では年間3.3万人が死亡していると推定されています。対策を採らないと2050年には世界で1000万人が薬剤耐性菌に関連して亡くなるという予測があるほどです。抗生物質がすぐに効かなくなる薬剤耐性菌は深刻な問題なのです。
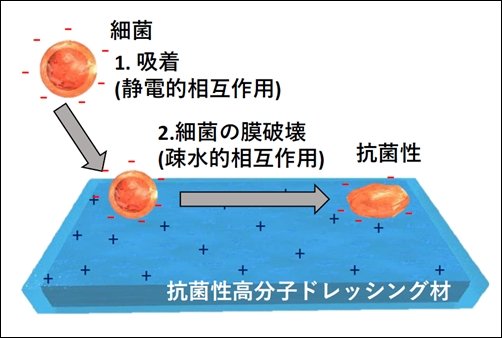
試作したドレッシング材が抗菌性を示すメカニズム
では薬剤耐性菌に対して、高分子化学の研究者はどう立ち向かえばよいのでしょうか。そこに医療現場からの声がありました。「特に手術後の傷口や医療デバイスからの感染は、既存のドレッシング材では完全に防げない」。この声が抗菌機能を持つドレッシング材開発のスタートになりました。
開発したのは「菌を吸着し細菌の細胞膜を破壊する」高分子です。そのメカニズムも実にスマートです。高分子の表面に正電荷を持たせることで、負の電荷を持つ細菌を吸着します。そして細菌の細胞膜(脂質二重層)を、疎水基が乱すことで穴を開け、壊します。細胞膜はどの細菌も持っていますから、原理的にはほぼすべての細菌に効果のある方法です(※2)。
※2 細菌とウイルス:ウイルスは細胞膜を持たない。このためウイルスを壊す機能はない
正電荷と疎水基という両方の機能を持つ高分子シートを作り、その効果を評価しました。「例えば大腸菌はほとんど死滅することが分かりました」(小土橋准教授)。薬剤耐性菌への効果も認められました。特に、メチシリン耐性黄色ブドウ球菌(MRSA)と呼ぶ細菌は、薬剤耐性菌の代表的なものとして知られています。このMRSAに対しても、試作したドレッシング材は抗菌性を示すことが分かりました。
傷口に貼るだけで細菌の感染を防ぐシートの実現可能性が見えてきました。
開発したのは「菌を吸着し細菌の細胞膜を破壊する」高分子です。そのメカニズムも実にスマートです。高分子の表面に正電荷を持たせることで、負の電荷を持つ細菌を吸着します。そして細菌の細胞膜(脂質二重層)を、疎水基が乱すことで穴を開け、壊します。細胞膜はどの細菌も持っていますから、原理的にはほぼすべての細菌に効果のある方法です(※2)。
※2 細菌とウイルス:ウイルスは細胞膜を持たない。このためウイルスを壊す機能はない
正電荷と疎水基という両方の機能を持つ高分子シートを作り、その効果を評価しました。「例えば大腸菌はほとんど死滅することが分かりました」(小土橋准教授)。薬剤耐性菌への効果も認められました。特に、メチシリン耐性黄色ブドウ球菌(MRSA)と呼ぶ細菌は、薬剤耐性菌の代表的なものとして知られています。このMRSAに対しても、試作したドレッシング材は抗菌性を示すことが分かりました。
傷口に貼るだけで細菌の感染を防ぐシートの実現可能性が見えてきました。
課題はコスト、10年後に実用を目指す
抗菌性を持つ高分子ドレッシング材は多くの関心を集めています。プロトタイプ開発についての研究は、特許取得や学術論文に掲載されて注目されているほか、新聞やテレビ、雑誌に取り上げられました。
小土橋准教授は「ドレッシング材の市場は世界で1兆円規模と予測されています。新開発のドレッシング材は薬剤耐性菌に対しても抗菌性があり、既存のドレッシング材と入れ替わる可能性を持っています。今後、国内の企業と連携して医療機器として市場に参入することを目指しています」と意気込みを口にします。
ただし、開発中の機能性高分子にも、まだ実用化に向けて解決しなければならない課題があります。その一つがコストですが、「コストの課題は構造を工夫することで解決できると考えています」。コストを含め、実用化のメドは10年後と見ています。
小土橋准教授の研究が人類を救う。その未来が少しずつ近づいています。
小土橋准教授は「ドレッシング材の市場は世界で1兆円規模と予測されています。新開発のドレッシング材は薬剤耐性菌に対しても抗菌性があり、既存のドレッシング材と入れ替わる可能性を持っています。今後、国内の企業と連携して医療機器として市場に参入することを目指しています」と意気込みを口にします。
ただし、開発中の機能性高分子にも、まだ実用化に向けて解決しなければならない課題があります。その一つがコストですが、「コストの課題は構造を工夫することで解決できると考えています」。コストを含め、実用化のメドは10年後と見ています。
小土橋准教授の研究が人類を救う。その未来が少しずつ近づいています。
研究者プロフィール
小土橋陽平 准教授
物質生命科学科
2011年 鹿児島大学大学院 理工学研究科 博士課程修了
2011年 アルバータ大学 化学/物質工学科 博士研究員
2013年 物質・材料研究機構(NIMS) WPI-MANA ICYS研究員
2016年 静岡理工科大学 理工学部 物質生命科学科 講師
2020年 現職
物質生命科学科
2011年 鹿児島大学大学院 理工学研究科 博士課程修了
2011年 アルバータ大学 化学/物質工学科 博士研究員
2013年 物質・材料研究機構(NIMS) WPI-MANA ICYS研究員
2016年 静岡理工科大学 理工学部 物質生命科学科 講師
2020年 現職

